
小編帶你看好宅
位於台北市天母,以俐落的現代風為主軸的牙醫診所,設計師以質感的灰階色調鋪敘色彩基底,襯托出窗外的清新陽光和綠意,即便在診療時,也能享受戶外的街道風景,更擴大了整體的空間感後,紓緩看牙醫時的緊張感,感受悠閒自在的環境氛圍。
走進診所後,迎面而來的是意想不到開闊空間感,櫃台區結合不規則的俐落造型設計、玻璃吊燈,和大面積的灰鏡材質,賦予時尚現代的品牌個性;並以灰階的黑白色調使用,給予沉穩與值得信賴的專業感。
接待區置入一張咖啡色的皮革沙發,以柔軟的質感和帶有暖度的色調,營造時髦而富有溫度的休憩空間。診療區安排於落地玻璃窗旁,使明亮的陽光得以洋溢室內空間,亦可觀賞戶外的樹景綠意,並在簡潔冷冽的色調中,注入屬於大自然的溫度和生命力。
隨著時序的切換,來到夜晚時分,外部大幅的落地窗如同精品專櫃的展示玻璃櫥窗,搭配簡約的梯階格塊和灰色的水磨石紋理,展現低調而精緻的氣質底蘊。
小編的最愛
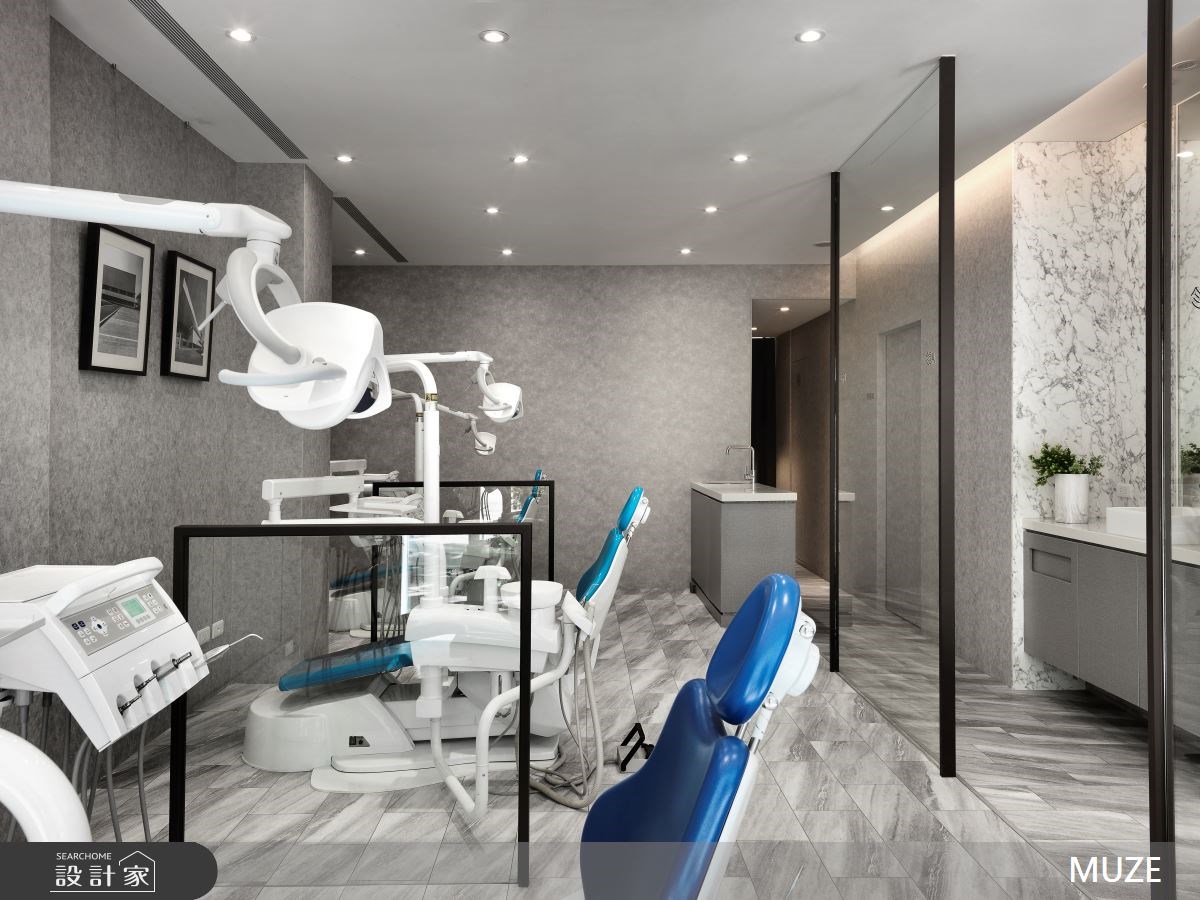
為了不影響採光和空間感,在各個領域的界定規劃上,設計師運用清玻璃搭配黑色的框架打造清透的隔間屏風,同時也利用地坪的高度差和地磚的序列方向,做為隱性的空間劃分。







原文轉載來自:源鏈接


